

Imagina tener la llave para acceder a un mercado de más de 450 millones de personas. Un mercado con altos estándares de calidad, una atención sanitaria de primer nivel y consumidores dispuestos a adoptar innovaciones tecnológicas. Esa llave existe y es el «marcado CE». Pero, ¿qué tiene que ver esto con el software sanitario y las apps médicas? Os invitamos a seguir leyendo para descubrirlo.
El marcado CE no es simplemente un logotipo que se pega en la caja de tu producto. Es una declaración que certifica que tu software o app médica cumple con los rigurosos estándares de calidad, seguridad y eficacia exigidos por la Unión Europea. Así mismo, también confirma que el medical device (en este caso el software) realmente funciona y cumple el objetivo para el que ha sido diseñado.
En el ámbito del software sanitario y las apps médicas, el marcado CE adquiere una relevancia excepcional. Estamos hablando de productos que podrían afectar la salud y el bienestar de las personas. Por lo tanto, las autoridades sanitarias son especialmente escrupulosas en asegurarse de que cualquier software o app que entre al mercado cumpla con los más altos estándares.
Así que, si estás pensando en lanzar tu software sanitario o app médica en el mercado europeo, este artículo es para ti. Vamos a desgranar paso a paso cómo obtener el marcado CE que te permitirá acceder con garantías a uno de los mercados más exigentes del mundo.
El marcado CE es como el pasaporte europeo para tus productos y, en este caso, un software sanitario o app médica. Estas dos letras, que significan «Conformidad Europea», son la garantía de que tu producto cumple con una serie de normativas y requisitos legales estipulados por la Unión Europea. Pero, ¿qué implica exactamente?
El marcado CE es un indicador de conformidad que certifica que un producto cumple con las directrices y normativas de la Unión Europea relacionadas con la seguridad, la salud y la protección medioambiental. Este marcado no solo es obligatorio para comercializar productos dentro del Espacio Económico Europeo (EEE), sino que también es un reconocimiento de calidad y seguridad que se valora en mercados de todo el mundo.
La Unión Europea no es solo un conglomerado de países, sino que también es un gigantesco mercado unificado con regulaciones armonizadas. Tener el marcado CE es la llave que te permite acceder a este mercado de más de 450 millones de consumidores. Pero hay que tener en cuenta que es un mercado que valora la calidad, la innovación y, sobre todo, muy exigente para asegurar la seguridad en productos sanitarios.
En el caso del software sanitario y las apps médicas, el marcado CE es aún más crucial, si cabe. Estos productos tienen un impacto directo en la salud y el bienestar de las personas, lo que significa que las autoridades están especialmente interesadas en garantizar que sean seguros, eficaces y de alta calidad. Al obtener el marcado CE, no solo te aseguras de cumplir con los requisitos legales, sino que también ganas la confianza de los consumidores y los profesionales de la salud, un aspecto invaluable para cualquier empresa en el sector sanitario.
Entonces, si estás planeando dar el salto al mercado europeo, no puedes ignorar la importancia del marcado CE. Es el sello que valida tu entrada en un mercado lleno de oportunidades pero también de responsabilidades.
Entrar al mercado de la Unión Europea consiste en cumplir con un conjunto de regulaciones y normativas que garantizan que tu software sanitario o app médica está a la altura de los estándares europeos. Pero no te preocupes, vamos a desglosar las regulaciones y normativas más importantes que debes tener en cuenta.

Empecemos por el Reglamento de Dispositivos Médicos de la Unión Europea (MDR 2017/745) y el Reglamento de Dispositivos de Diagnóstico In Vitro (IVDR 2017/746). Estas son las piedras angulares de la regulación de productos sanitarios en la UE. Aunque originalmente se centraban en dispositivos físicos, su alcance se ha ampliado para incluir software sanitario y apps médicas, quedando recogidos ahora en la definición de un medical device software. Antes de iniciar un proceso de obtención del marcado CE europeo, asegúrate que tu app es un medical device y no una app de wellness, learning u otras actividades relacionadas con la salud o el bienestar. Es crucial que te familiarices con estos reglamentos, ya que establecen los requisitos esenciales de seguridad y rendimiento que tu producto debe cumplir.
La ISO 14971 es la norma internacional para la gestión de riesgos en dispositivos médicos, y la IEC 62304 es la norma para el ciclo de vida del software de dispositivos médicos. Ambas son fundamentales para demostrar que has abordado de manera adecuada los riesgos asociados con tu software o app. En otras palabras, son tu manual para crear un producto no solo innovador, sino también seguro y eficaz.
Si tu software sanitario o app médica maneja datos personales, que es muy probable, tendrás que cumplir con el Reglamento General de Protección de Datos (RGPD) y la Ley Orgánica de Protección de Datos y Garantía de los Derechos Digitales (LOPD-GDD). Estas leyes protegen la privacidad de los datos y te obligan a implementar medidas de seguridad robustas. Además, la Ley de Autonomía del Paciente establece los derechos y obligaciones en cuanto al proceso informativo y la documentación clínica, algo especialmente relevante si tu app o software interactúa directamente con pacientes.
El camino hacia el marcado CE está lleno de requisitos legales y normativos que podrían parecer abrumadores al principio. Sin embargo, cada uno de ellos tiene un propósito: asegurarse de que los productos que llegan al mercado europeo sean seguros, eficaces y respeten la privacidad y los derechos de los usuarios. Al final del día, cumplir con estas normativas no solo te permitirá obtener el marcado CE, sino que también te brindará un sello de calidad y confianza que te distinguirá en el mercado.
Una vez sabemos qué regulaciones y normativas se deben tener en cuenta, es hora de abordar el «cómo». Obtener el marcado CE no es una tarea sencilla, pero como en todo proceso, resulta más fácil cuando lo desglosamos en pasos más pequeños. A continuación os guiamos en ese proceso, paso a paso.

La evaluación de conformidad es el pilar fundamental en el proceso de obtención del marcado CE para un software sanitario o app médica. Este paso inicial es crucial para determinar si el producto está listo para acceder al mercado de la Unión Europea o si necesita ajustes significativos. A continuación, os mostramos un análisis exhaustivo de qué implica este proceso y cómo te puedes preparar de manera efectiva.
Comprendiendo la Importancia
Antes de entrar en los aspectos técnicos, es vital entender la importancia de la evaluación de conformidad. Este proceso no solo evalúa si tu producto cumple con las normas y regulaciones de la UE, sino que también sirve como una auditoría integral de la calidad, la seguridad y la eficacia de tu software sanitario o app médica. En resumen, es la primera y más crucial barrera que debes superar para ganar la confianza de las autoridades y, finalmente, de los usuarios finales.
Elección del Procedimiento de Evaluación
Existen diferentes procedimientos de evaluación de conformidad, y la elección del más adecuado depende del tipo de software sanitario o app médica que estés desarrollando. Para algunos productos, una autoevaluación podría ser suficiente, mientras que otros podrían requerir una evaluación más detallada por parte de un organismo notificado. Es importante investigar cuál es el más adecuado para cada caso y prepararse en consecuencia.
Análisis de Requisitos Específicos
El siguiente paso es realizar un análisis en profundidad de los requisitos específicos que el producto debe cumplir según las normativas y regulaciones pertinentes, como MDR 2017/745 o IVDR 2017/746. Este análisis debe ser meticuloso e incluir aspectos como funcionalidad, seguridad, protección de datos y demás. Es importante no escatimar esfuerzos en este paso, ya que cuanto más detallado sea el análisis, más sencillo resultará el resto del proceso.
Realización de Pruebas Preliminares
Antes de centrar los esfuerzos en preparar la documentación técnica, es recomendable realizar pruebas preliminares para evaluar cómo se alinea el producto con los requisitos identificados. Esto te dará una idea clara de las áreas que necesitan mejora y te permitirá corregir cualquier deficiencia antes de avanzar.
Compilación de Evidencia
Toda la evidencia recopilada durante este proceso debe documentarse de manera clara y coherente. Esto incluye los resultados de tu análisis de requisitos, las pruebas preliminares y cualquier otra evaluación que hayas realizado. Esta documentación será crucial más adelante, por lo que es fundamental que sea completa y esté bien organizada.
Evaluación por Terceros (Si es Necesario)
Si tu producto cae en una categoría que requiere de la intervención de un organismo notificado, deberás preparar la documentación para una revisión externa. Este organismo evaluará si tu evaluación de conformidad ha sido exhaustiva y si tu producto cumple con todos los requisitos necesarios.
Retroalimentación y Ajustes
Independientemente del resultado, la evaluación de conformidad te proporcionará una retroalimentación que podrás usar para hacer ajustes y mejoras. Toma este feedback en serio y utilízalo para elevar la calidad y la conformidad de tu producto.
En pocas palabras
La evaluación de conformidad es un proceso multifacético que requiere una planificación cuidadosa, una ejecución meticulosa y una documentación rigurosa. No es una tarea que deba tomarse a la ligera, ya que establece el tono para todo el proceso de obtención del marcado CE.
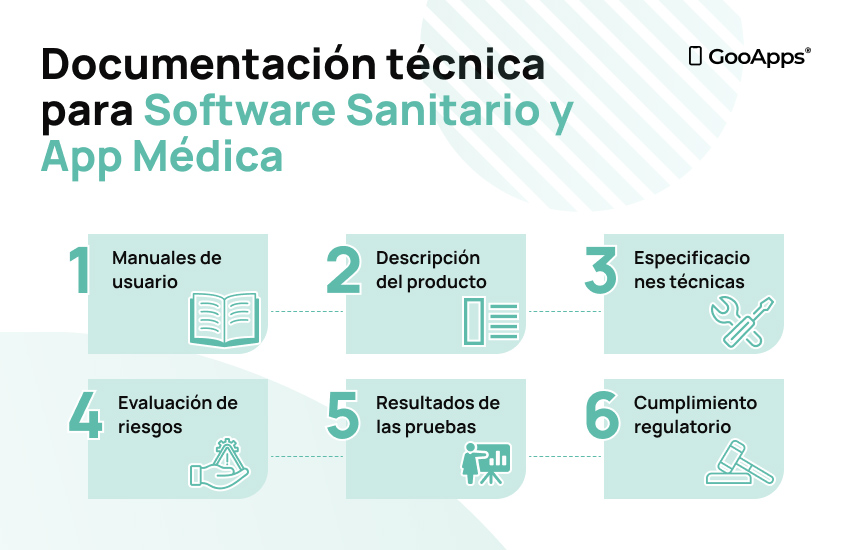
Si la evaluación de conformidad es el pilar fundamental en el proceso de obtención del marcado CE, entonces la documentación técnica es, sin duda, el núcleo. Aquí es donde se consolida todo el trabajo previo, y se presenta de manera organizada y coherente para demostrar que tu software sanitario o app médica está listo para el mercado europeo.
Pero, antes de profundizar en este apartado, es importante entender que solo necesitamos el marcado CE cuando la app o software tiene que cumplir con las características de un SaMD (Software as a Medical Device). La definición dice lo siguiente:
“Un SaMD recoge múltiples datos de entrada, como resultados de laboratorio, síntomas del paciente o datos de imágenes médicas, y los procesa utilizando varios tipos de algoritmos. El software entonces produce resultados que se utilizan para diversos fines médicos, incluyendo ayudar a los usuarios a diagnosticar, tratar y gestionar sus problemas de salud.”
La mayoría de apps de salud, bienestar y deporte no son un medical device, por lo que no tienen que cumplir por lo que se exige en un SaMD.
Ahora bien, si nuestro software sanitario o app médica sí que actúa como un SaMD, entonces vamos a explorar en profundidad qué implica este paso crucial.
¿Qué es la Documentación Técnica?
La documentación técnica es un conjunto comprensivo de documentos que aportan evidencia objetiva para demostrar que tu producto cumple con todos los requisitos y regulaciones necesarias, y con la función que dice cumplir en su objetivo de creación. En otras palabras, es tu cartera de pruebas que respalda la seguridad, eficacia y calidad de tu software sanitario.
Componentes Clave
La documentación técnica se compone de varios elementos, y cada uno tiene su importancia. Estos suelen incluir:
En la regulación MDR 2017/745 y IVDR 2017/746 quedan recogidos y detallados todos estos requisitos.
Preparación y Organización
La preparación de la documentación técnica requiere un enfoque metódico. Asegúrate de que cada documento esté completo, preciso y actualizado. La organización también es clave, ya que un dossier desorganizado puede llevar a retrasos innecesarios durante el proceso de revisión.
Validación por Expertos
Antes de enviar tu documentación, es altamente recomendable que pase por un proceso de validación por parte de expertos en el campo. También se recomienda que, al menos la primera vez, te asesores con expertos para preparar esta documentación inicialmente y evitarte sorpresas en la primera auditoría del organismo notificado (una organización designada por un país de la UE para evaluar la conformidad de ciertos productos antes de ser introducidos en el mercado). Esto puede incluir asesoramiento legal para el cumplimiento regulatorio, consultas con ingenieros de software para la precisión técnica, y opiniones de profesionales de la salud para la aplicabilidad clínica.
Documentación Adicional
No subestimes la importancia de añadir cualquier documentación adicional que pueda fortalecer tu caso. Esto puede incluir estudios de caso, testimonios de expertos en el campo, o cualquier otro material que pueda respaldar la eficacia, funcionalidad y seguridad de tu producto.
En definitiva
La documentación técnica es una etapa que requiere una atención meticulosa al detalle. Es el compendio de tu trabajo y esfuerzo, presentado de una forma que demuestre de manera concluyente que tu software sanitario o app médica satisface todos los requisitos para obtener el marcado CE. Dada su importancia, este es un paso en el que la precisión, la exhaustividad y la claridad son absolutamente cruciales.

Tras haber presentado la evaluación de conformidad y la documentación técnica, los ensayos y pruebas son la fase donde demostrar en la práctica que tu software sanitario o app médica cumplen con lo indicado en los puntos anteriores. Este es el escenario donde tu producto es sometido a una serie de evaluaciones que medirán su calidad, funcionalidad, seguridad y eficacia. A continuación, profundizamos en este tercer paso.
La Importancia de los Ensayos y Pruebas
Los ensayos y pruebas son la confirmación empírica de que tu producto es apto para su propósito. Este es el momento donde todas las afirmaciones que has hecho en tu documentación técnica se ponen a prueba. No hay lugar para la ambigüedad, por lo que los resultados de estos ensayos serán un factor determinante en la obtención del marcado CE.
Tipos de Ensayos y Pruebas
Dependiendo del tipo y complejidad de tu software sanitario o app médica, podrás enfrentarte a una variedad de pruebas, que pueden incluir:
Protocolo de Pruebas
Es fundamental que diseñes un protocolo de pruebas riguroso que detalle cómo se llevarán a cabo cada una de las pruebas, qué criterios se utilizarán para evaluar los resultados y cómo se documentará todo. Este protocolo servirá como guía durante todo el proceso y como una evidencia adicional de la meticulosidad de tu enfoque.
Documentación de Resultados
Cada prueba y ensayo que realices debe ser meticulosamente documentado. Los resultados, tanto positivos como negativos, se añadirán a tu documentación técnica y serán esenciales para el proceso de revisión posterior.
Análisis y Ajustes
Una vez concluidos los ensayos y pruebas, es crucial hacer un análisis detallado de los resultados. Si se identifican deficiencias o áreas de mejora, este es el momento para hacer los ajustes necesarios. No veas los fallos como un retroceso, sino como oportunidades para mejorar y optimizar tu producto.
En Resumen
Los ensayos y pruebas son la fase en la que se demuestra la calidad de tu software sanitario o app médica. Es un proceso que requiere una planificación cuidadosa, una ejecución precisa y un análisis crítico. Y aunque puede ser un camino lleno de desafíos, también es una oportunidad inigualable para demostrar que tu producto está a la altura de los estándares más exigentes.
Es muy importante que planifiques y asegures que podrás realizar estas pruebas en hospitales, centros de salud, etc. y no dejar para el último momento la búsqueda de estos contactos que te ayudarán en esta fase de la verificación. Muchas veces, se llega a este punto y no se dispone de centros para el test del producto, lo que resulta en el proyecto quedando bloqueado sin poder avanzar.
Antes de presentar la documentación de forma oficial, es recomendable realizar una auditoría interna para asegurar que todo está en conformidad. Si fuera necesario aplicar cambios, siempre es más conveniente realizar las mejoras antes de la presentación formal a las agencias.
Una vez estés totalmente seguro de la conformidad de la documentación, estarás listo para el proceso de revisión, que es el examen final que determinará si tu software sanitario o app médica están listos para recibir el marcado CE. Este es un momento crítico donde un organismo notificado examina toda la documentación, pruebas y evidencias que has reunido, para tomar una decisión informada sobre la conformidad de tu producto. Veamos en detalle este apartado.
La Naturaleza del Proceso de Revisión
El proceso de revisión es una evaluación exhaustiva llevada a cabo por un organismo notificado, que es una entidad independiente acreditada por las autoridades de la Unión Europea para evaluar la conformidad de productos sanitarios. El objetivo es simple pero fundamental: asegurarse de que tu software sanitario cumpla con todos los requisitos y normativas necesarias para garantizar su seguridad y eficacia.
Preparación para la Revisión
La preparación para este proceso es esencial. Asegúrate de que tu documentación técnica esté completa, bien organizada y fácil de seguir. Cada detalle cuenta. Un dossier incompleto o desordenado podría retrasar la revisión y, en el peor de los casos, resultar en un fallo en la evaluación.
La Revisión en Detalle
Durante el proceso de revisión, el organismo notificado examinará meticulosamente cada pieza de documentación que has presentado. Esto incluirá, pero no se limitará a:
Tiempos y Plazos
Es difícil dar un marco de tiempo exacto para el proceso de revisión, ya que esto dependerá de la complejidad de tu software o app médica, así como del volumen de documentación a revisar. Sin embargo, es crucial ser proactivo y responder rápidamente a cualquier solicitud de información adicional o aclaraciones por parte del organismo notificado.
Posibles Resultados y Pasos Posteriores
Los resultados de la revisión pueden variar. En el mejor de los casos, tu producto recibirá la aprobación para el marcado CE sin condiciones. Sin embargo, es posible que se requieran ajustes o que debas proporcionar información adicional. En casos excepcionales, tu solicitud podría ser rechazada, lo que generalmente te obligará a revisar y ajustar significativamente tu producto y documentación.
Al fin y al cabo
El proceso de revisión es el último paso para obtener el marcado CE. Es una fase que requiere una atención meticulosa al detalle y una preparación exhaustiva. Recuerda que este es el momento donde todo tu trabajo previo se somete a escrutinio, y la calidad y conformidad de tu producto se evalúan de manera definitiva.
Si el proceso de revisión resulta satisfactoria, significa que has llegado el paso final para la obtención del marcado CE: la certificación. Si bien este momento podría parecer simplemente como una formalidad, en realidad es más que eso. La certificación no solo representa la culminación de todo tu arduo trabajo, sino que también abre la puerta a nuevas responsabilidades y oportunidades. Aquí te detallamos qué implica esta etapa y cómo puedes prepararte para ella.
Obtención del Certificado
Una vez que el organismo notificado haya revisado y aprobado toda tu documentación, ensayos y pruebas, te otorgará un certificado de conformidad. Este es el documento que oficialmente te permite añadir el marcado CE a tu software sanitario o app médica, señalando que cumple con todas las normativas y estándares europeos.
¿Qué Incluye el Certificado?
El certificado de conformidad generalmente incluirá detalles como el nombre del producto, la versión del software, el nombre y la dirección del fabricante (o sea, tu empresa), y una descripción detallada de las funciones y características del producto. También contendrá información sobre las normativas y estándares específicos que el producto cumple.
Validación y Vigencia
Es importante notar que la certificación no es un cheque en blanco. Generalmente tiene un período de vigencia, tras el cual deberá ser renovada. Además, si realizas cambios significativos en el software o en la app, como añadir nuevas funcionalidades o modificar su estructura, podrías necesitar pasar por un proceso de reevaluación.
Auditorías y Seguimiento
Obtener el marcado CE no es el final del camino, sino más bien el comienzo de una nueva fase. Serás sujeto a auditorías periódicas para asegurarse de que tu producto sigue cumpliendo con los estándares y normativas. Estas auditorías pueden ser tanto anunciadas como no anunciadas, por lo que es crucial mantener un nivel constante de calidad y conformidad.
Compromiso Continuo con la Calidad
La certificación implica asumir también un compromiso continuo con la calidad, la seguridad y la eficacia de tu producto. La reputación de tu software o app no solo dependerá del marcado CE, sino también de cómo respondes a los comentarios de los usuarios, cómo gestionas los problemas y cómo te adaptas a las nuevas regulaciones o tecnologías emergentes.
En conclusión
La certificación es el último hito en el proceso de obtención del marcado CE, pero también es un recordatorio de la importancia de mantener un enfoque constante en la calidad y la conformidad. Es tanto un reconocimiento de tu éxito hasta el momento como un desafío para seguir cumpliendo con los más altos estándares en el futuro.
En la era digital en la que vivimos, las apps médicas están ganando terreno rápidamente como herramientas efectivas para la atención sanitaria. Sin embargo, es crucial entender que aunque estas apps puedan considerarse una subcategoría del software sanitario, tienen sus propias particularidades y, por lo tanto, requisitos específicos para la obtención del marcado CE. En este apartado, vamos a explorar estas diferencias en detalle.
Las apps médicas, aunque similares en muchos aspectos al software sanitario tradicional, tienen sus propias particularidades que requieren una atención especial durante el proceso de certificación para el marcado CE. Desde la plataforma de uso hasta la interacción del usuario y el manejo de datos sensibles, es vital considerar estos elementos únicos para asegurar no solo la obtención del marcado CE, sino también el éxito y la aceptación de la app en el mercado.
Hasta ahora, nos hemos centrado en el proceso y los requisitos para obtener el marcado CE en software sanitario y apps médicas. Pero, ¿qué ventajas ofrece a tu producto y a tu empresa? A continuación, exploramos los múltiples beneficios que acompañan a la obtención del marcado CE.
Obtener el marcado CE no es solo una cuestión de cumplimiento regulatorio, sino una inversión estratégica que ofrece múltiples beneficios, desde el acceso a nuevos mercados hasta la construcción de una marca de confianza y la obtención de ventajas competitivas. En un mundo donde la calidad y la confianza son más valoradas que nunca, el marcado CE sirve como un sello de excelencia que puede impulsar el éxito de tu software sanitario o app médica. Obtener el marcado CE requiere una gran inversión de tiempo y recursos, pero solo hay que realizar el proceso una sola vez. Tras haberlo obtenido, sólo se tendrán que realizar ciertas acciones de seguimiento a lo largo de los años.
Obtener el marcado CE es un logro significativo que abre numerosas puertas, pero el camino para llegar hasta su obtención no está exento de obstáculos. Es un proceso complejo que requiere una planificación cuidadosa, recursos y un compromiso total con la calidad y la conformidad. En esta sección, exploraremos algunos de los desafíos más comunes con los que te podrías enfrentar y cómo GooApps puede ayudarte a superarlos.
Obtener el marcado CE es una tarea compleja llena de desafíos. Sin embargo, con el apoyo adecuado y una planificación cuidadosa, estos obstáculos son totalmente superables. En GooApps, te ofrecemos la experiencia, los recursos y el compromiso necesarios para hacer de este proceso no solo un trámite exitoso sino una inversión en el futuro de tu software sanitario o app médica.
Si has llegado hasta aquí, seguramente tienes una comprensión completa y detallada de la importancia y el proceso para obtener el marcado CE en software sanitario y apps médicas. Este símbolo es la llave que abre las puertas a un mercado de más de 450 millones de personas en la Unión Europea, y es un sello de calidad y confianza que puede diferenciar tu producto en un mercado cada vez más competitivo.
El camino hacia el marcado CE es complejo y lleno de desafíos. Pero la buena noticia es que no tienes que hacerlo solo.
¿Necesitas ayuda para obtener el marcado CE para tu software sanitario o app médica? GooApps está aquí para ayudarte.
Contamos con un equipo multidisciplinario de expertos que pueden guiarte en cada paso del proceso, desde la evaluación de conformidad hasta la certificación final, asegurando que tu producto cumpla con todas las normativas y estándares necesarios.
Completa el formulario y GooApps® te ayudará a encontrar la mejor solución para tu organización. ¡Contactaremos contigo muy pronto!